B-celdepletie en anti-CD20-antilichamen bij MS [1]
Selectieve B-celdepletie aan de hand van monoklonale antilichamen die selectief zijn gericht tegen CD20 is een veelbelovende nieuwe behandeling bij MS gebleken. De hoge effectiviteit ervan is bovendien een empirische bevestiging van de centrale rol van B-cellen bij de pathogenese van MS. Hoe de effectiviteit van B-celdepletie bij MS behaald wordt is echter nog niet precies verklaard.
CD20 als target bij B-celdepletie
CD (cluster of differentiation)-moleculen zijn een onderdeel van een groep van oppervlaktemoleculen die tot expressie komen op cellen van het afweersysteem. Veelal spelen CD-moleculen een sleutelrol bij de communicatie tussen cellen, maar in sommige gevallen kunnen ze ook betrokken zijn bij andere processen, zoals celadhesie. Het zijn essentiële markers voor de fenotypering van leukocyten en bepaalde categorieën lymfocyten. CD20 is een oppervlaktemolecuul dat in verschillende ontwikkelingsstadia van de B-cel tot expressie komt: vanaf het stadium van de late pre-B-cel tot dat van plasmablast; de vroege plasmacel en de geheugen B-cel. CD20 speelt een belangrijke functionele rol bij de activering, proliferatie en differentiatie van B-cellen.
Tegen B-cellen gerichte behandeling van MS is sterk tot ontwikkeling aan het komen, sinds is onderkend dat depletie van CD20-positieve (CD20+) B-cellen in de circulatie gunstige effecten heeft op klinische en beeldvormende parameters.9 Deze behandeling beïnvloedt alle eerdergenoemde pathogene mechanismen van B-cellen, zowel bij MS als bij een veelgebruikt diermodel voor MS: experimentele autoimmuun-encefalomyelitis (EAE). Tevens is met name uit de off-label behandeling van MS met rituximab, een chimeer anti-CD20 antilichaam, bewijs gekomen dat de B-cel in de periferie een belangrijke rol speelt als APC.19,20 Let wel, in het CZS heeft de plasmacel wel degelijk een belangrijke rol als antilichaam producerende cel.
Momenteel zijn in Europa twee monoclonale anti-CD20 antilichamen beschikbaar voor de behandeling van MS; het volledig humane antilichaam ofatumumab (s.c.) en het gehumaniseerde antilichaam ocrelizumab (i.v.).42, 43 Tegen CD20 gerichte monoklonale antilichamen binden aan het CD20-oppervlakte-eiwit. Ze veroorzaken in de perifere circulatie, het beenmerg, de milt en de perifere lymfeklieren selectieve depletie van CD20+ B-cellen: dat zijn pre-B-cellen, volgroeide B-cellen en memory B-cellen. Hematopoëtische stamcellen in het beenmerg en antilichaam-producerende plasmacellen blijven buiten schot.
Door anti-CD20-therapie gemedieerde B-celdepletie wordt volgens de laatste inzichten geïnduceerd door vier mechanismen:
- antilichaam-afhankelijke cellulaire cytotoxiciteit (ADCC);
- antilichaam-afhankelijke cellulaire fagocytose (ADCP);
- complement-afhankelijke cytotoxiciteit (CDC);
- directe apoptose.
Meer hierover vindt u op de pagina over monoclonale antilichamen [2].
Antilichamen tegen CD20 onderdrukken de inflammatoire ziekteactiviteit in hoge mate en worden gezien als een belangrijke nieuwe stap voorwaarts bij de behandeling van MS. Opvallend is dat deze therapeutische benadering niet alleen effectief is bij RRMS, maar ook bescherming lijkt te bieden tegen het verergeren van beperkingen bij PPMS.

Andere behandelingen met B-cellen als target
Steeds duidelijker wordt dat B-cellen een centrale rol spelen bij het werkingsmechanisme van MS-medicijnen. De meeste bestaande behandelingen voor RRMS zijn oorspronkelijk ontworpen om T-cellen te targetten, maar van de meeste hiervan is inmiddels duidelijk dat ze daarnaast ook B-cellen als target hebben.11 Enkele voorbeelden hiervan binnen het huidige behandellandschap van MS zijn:
- natalizumab22, een selectieve adhesie molecuulremmer. Dit anti-α4-integrine oftewel een anti-VLA-4 antilichaam voorkomt transmigratie van zowel T- als B-lymfocyten over de BHB het parenchym in;
- alemtuzumab23, een anti-CD52 antilichaam dat zowel volwassen T- als B-cellen in de bloedsomloop elimineert;
- cladribine24, een analoge purine nucleoside anti-metaboliet die zorgt voor DNA-schade en daaruit voortvloeiende apoptose (celdood) van geactiveerde B- en T-cellen;
- fingolimod25, siponimod26 en ozanimod27, selectieve S1PR modulatoren die voornamelijk geactiveerde T-, maar ook B-lymfocyten gevangen houden in de lymfeknoop en daarmee voorkomen dat er circulatie is van pathogene effector immuuncellen;
- Dimethyfumaraat28; werkt door activering van het eiwit “Nrf2”, een transcriptiefactor betrokken bij de regulering van de bescherming tegen oxidatieve stress. Gebleken is dat dimethylfumaraat ontstekingen vermindert en de activiteit van het immuunsysteem moduleert;
- Bruton's tyrosinekinase (BTK) remmers. Het enzym BTK speelt een centrale rol bij het activeren van B-cellen wanneer de B-celreceptor gebonden wordt met een antigen. Er zijn meerdere BTK-remmers in ontwikkeling voor de behandeling van MS. Ze remmen de activatie van B-cellen en de interactie tussen B- en T-cellen. Huidig zijn de BTK remmers in ontwikkeling voor de behandeling van MS door meerdere geneesmiddelfabrikanten.
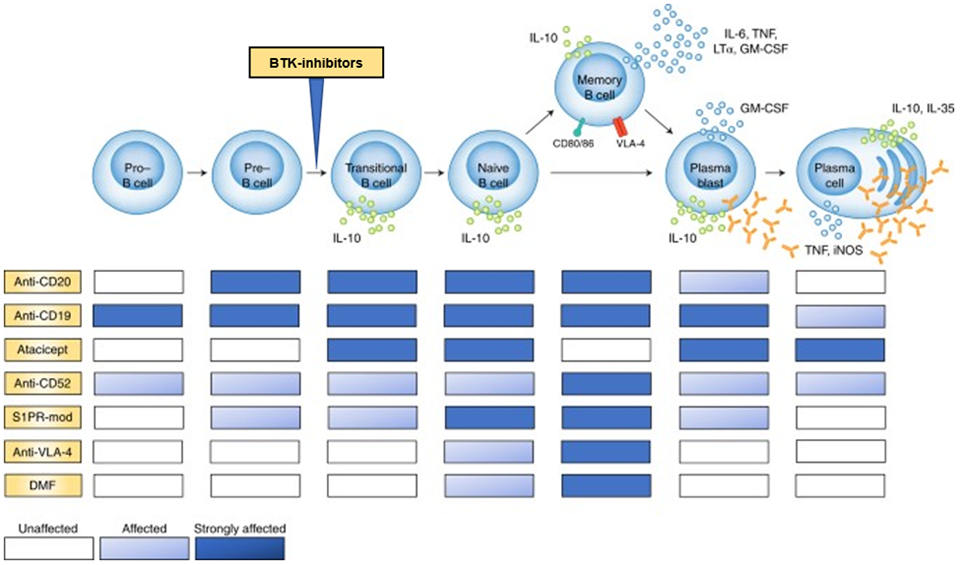
Adapted from Li et al., Nature Immunol 2018